更多功能
特瑞普利单抗注射液
特瑞普利单抗 Toripalimab 拓益
240mg/6ml 80mg/2ml
本品适用于既往接受全身系统治疗失败的不可切除或转移性黑色素瘤的治疗。
*本品适用于含铂化疗失败包括新辅助或辅助化疗12个月内进展的局部晚期或转移性尿路上皮癌的治疗。
*以上适应症在中国是基于单臂临床试验的客观缓解率结果给予的附条件批准。
本适应症的完全批准将取决于正在开展中的确证性临床试验能否证实中国患者的长期临床获益。
本品适用于既往接受过二线及以上系统治疗失败的复发/转移性鼻咽癌患者的治疗。
本品联合顺铂和吉西他滨用于局部复发或转移性鼻咽癌患者的一线治疗。
本品联合紫杉醇和顺铂适用于不可切除局部晚期/复发或转移性食管鳞癌的一线治疗。
本品须在有肿瘤治疗经验医生的指导下用药。
推荐剂量
二线黑色素瘤、二线尿路上皮癌、二线鼻咽癌(单药治疗):推荐剂量为3mg/kg,静脉输注每2周一次,直到疾病进展或出现不可耐受的毒性。
局部复发或转移性鼻咽癌一线、不可切除的局部晚期/复发或转移性食管鳞癌一线:本品推荐剂量为固定剂量240mg,静脉输注每3周一次,至疾病进展或发生不可耐受的毒性。
特瑞普利单抗联合化疗给药时,应首先给予特瑞普利单抗。另请参见化疗药物给药的处方信息。
已观察到接受本品治疗肿瘤的非典型反应(例如,治疗最初几个月内肿瘤出现暂时增大或者出现新的小病灶,随后肿瘤缩小)。如果患者临床症状稳定或持续减轻,即使有疾病进展的初步证据,基于总体临床获益的判断,可考虑继续应用本品治疗,直至证实疾病进展。
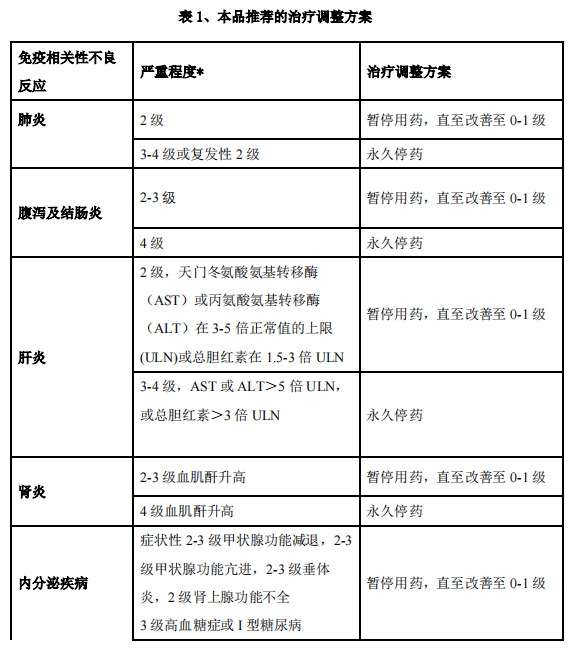
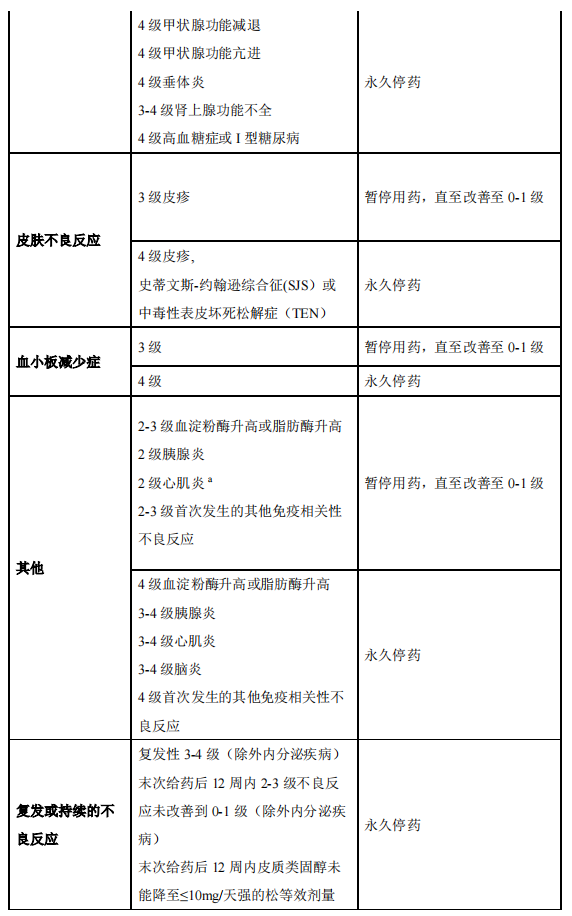
根据个体患者的安全性和耐受性,可能需要暂停给药或永久停用。不建议增加或减少剂量。暂停给药或永久停用的指南请见表1。有关免疫相关性不良反应管理的详细指南,请参见【注意事项】

特殊人群
肝损伤
本品在中度或重度肝功能损伤患者中使用的安全性及有效性尚未建立,不推 荐用于中、重度肝功能损伤的患者。轻度肝功能损伤患者应在医生指导下慎用本 品,如需使用,无需进行剂量调整。
肾损伤
本品在中度或重度肾功能损伤患者中使用的安全性及有效性尚未建立,不推 荐用于中、重度肾功能损伤的患者。轻度肾功能损伤患者应在医生指导下慎用本 品,如需使用,无需进行剂量调整。
儿童人群
尚未确立本品在 18 岁以下儿童及青少年中的安全性和有效性,无相关数据。
老年人群
老年人(65 岁及以上)建议在医生的指导下使用,无需进行剂量调整。
给药方法
本品首次静脉输注时间至少60分钟。如果第一次输注耐受性良好,则第二次 输注的时间可以缩短到30分钟。如果患者对30分钟的输注也具有良好的耐受性, 后续所有输注均可在30分钟完成。不得采用静脉推注或单次快速静脉注射给药。
给药前药品的稀释指导如下:
· 本品从冰箱取出后应在24小时内完成稀释液的配制。
· 配药前肉眼检查药品有无颗粒物以及颜色变化。本品为无色或淡黄色澄 明液体,可带轻微乳光。如观察到可见颗粒物或颜色异常应弃用药物。6
· 本品不含防腐剂,无菌操作下,抽取所需要体积的药物缓慢注入100 ml 生理盐水(0.9%氯化钠)输液袋中,配制成终浓度为1-3 mg/ml的稀释液, 轻轻翻转混匀,混匀后使用无菌过滤器(0.2或0.22 μm)静脉滴注。
· 无菌操作下配制的稀释液,室温下放置不超过8小时,这包括室温下贮存 在输液袋的时间以及输液过程的持续时间。在2~8℃下保存时间不超过 24小时。如果冷藏,请在给药前使稀释液恢复至室温。不得冷冻保存。
· 不可与其他药品混合或稀释。
· 药瓶中剩余的药物不可重复使用
同厂家
同功效